Все про углерод: опасность co2 и методы нейтрализации выбросов углекислого газа
Содержание:
- Что послушать
- Получение в промышленности
- Углекислый газ, формула, молекула, строение, состав, вещество:
- Углекислый газ и мы: чем опасен CO2
- Поглотители двуокиси углерода
- Химические и биологические свойства углекислого газа
- Методы регистрации
- Основные достоинства и недостатки пожаротушения углекислотой CO2
- Применение
- Токсичность
Что послушать
В новом эпизоде подкаста речь пойдет о том, что делать с ненужной одеждой, чем опасен текстиль на свалках и что такое свопы. Объем отходов модной индустрии в мире достигает 92 млн т в год, большая часть из них выбрасывается. На свалках одежда тлеет десятилетиями, выделяя метан и провоцируя пожары.
Чтобы этого избежать, необходимо перерабатывать ненужные вещи или отдавать их тем, кому они необходимы. О том, куда сдать текстиль, чтобы он не попал на свалку, расскажет Дарья Алексеева из фонда «Второе дыхание», который известен своими пунктами приема одежды и сетью магазинов Charity Shop.
Во второй части выпуска со-основательница проекта Swap it and never buy Наиля Гольман расскажет о свопах — еще одном способе подарить новую жизнь ненужным вещам.
Получение в промышленности
Получение диоксида углерода в промышленности методологически разнообразно. Он находится в дымовых отходах, выпускаемых в атмосферу ТЭЦ и электростанциями, получается при брожении спирта и выступает как продукт реакции с природными карбонатами.

Индустрия получения двуокиси углерода широка. Газ можно абсорбировать несколькими способами из одного источника. Во всех случаях это поэтапный процесс очистки от примесей (для достижения требований ГОСТа) и достижения нужной консистенции, агрегатного состояния.
Получение газообразной двуокиси углерода
Газообразный CO2 извлекают из промышленных (нефтяных) дымов путем адсорбции моноэтаноламина (коммерчески выгодно) и карбонатом калия (редко). Принцип сбора частиц углерода одинаков для обоих веществ. Они направляются по трубопроводу к отходам и собирают в себя углекислый газ. После сбора, насыщенные углекислотой газы направляются на очистку.
В специальных емкостях происходит реакция в при повышенной температуре или заниженном давлении. В процессе высвобождается чистая углекислота и продукты распада (аммиак и другие).
 Установка добычи углекислоты
Установка добычи углекислоты
Схематически процесс выглядит так:
- Отходящий дым смешивается с адсорбентами (газообразным карбонатом калия или моноэтаноламином);
- Накопившие в себе двуокись углерода газы поступают в специальный газгольдер для очистки;
- В реакции с высокой температурой или низким давлением происходит отделение углекислого газа от адсорбента.
В лаборатории извлечь много CO2 не получается. Но это возможно в реакции с гидрокарбонатами и кислотами. В отдельности CO2 можно выделить на промышленных станках для получения кислорода, аргона или азота. Углекислый газ здесь выступает как побочный продукт. Хранится он в специальных баллонах, поставляемых потребителю.
Получение жидкой углекислоты
Добыча жидкой углекислоты поэтапно связана с получением ее из газа. Из летучего газообразного состояния, при обработке водородом, раствором перманганата калия и углем, образуется жидкая двуокись.
Сжижение происходит из-за низкого давления, сопровождающего реакцию. После многоступенчатой очистки, жидкий диоксид углерода попадает в компрессор. Там он сжимается и подается для сушки в 2 адсорбера, поочередно перенимающие работу для восстановления. Параллельно сжатая жидкость очищается от запахов и переводится в конденсатор, а оттуда – на хранение.
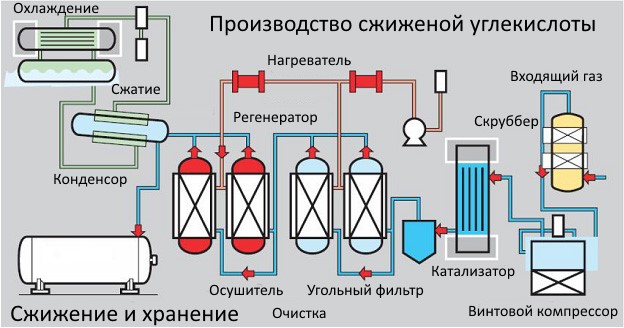
Этот метод сжижения применяется для газов спиртового брожения. Он актуален для пропана, бутана и т.д. Его используют на крупных пивоварнях, а получаемая очищенная углекислота имеет высокие показатели качества.
Получение твердого диоксида углерода
Твердый диоксид образуют из жидкого путем обработки низкой температурой (-56°). В промышленных условиях только 20% переходят в твердое состояние, а остальные – испаряются.
 Сухой лед
Сухой лед
Порядок извлечения углекислотных кристаллов (сухого льда):
- Из емкости брожения газ переходит в емкость для промывки;
- В газгольдере после мытья он сжимается и сжижается;
- Многократно сжимаясь и нагреваясь, газообразный углерод охлаждается в специальных холодильниках;
- Жидкость очищается активированным углем;
- Поступает в холодильник, где охлаждается и дополнительно очищается от примесей;
- Охлажденный CO2 направляется на испарение и пресс, где комплектуется сухой лед.
Углекислый газ, формула, молекула, строение, состав, вещество:
Углекислый газ (диоксид углерода, двуокись углерода, углекислота, оксид углерода (IV), угольный ангидрид) – бесцветный газ, почти без запаха (в больших концентрациях с кисловатым «содовым» запахом).
Углекислый газ – бинарное химическое соединение углерода и кислорода, имеющее формулу CO2.
Химическая формула углекислого газа CO2.
Строение молекулы углекислого газа, структурная формула углекислого газа:
Углекислый газ тяжелее воздуха приблизительно в 1,5 раза. Его плотность при нормальных условиях составляет 1,98 кг/м3, по отношении к воздуху – 1,524. Поэтому скапливается в низких непроветриваемых местах.
Концентрация углекислого газа в воздухе (в атмосфере Земли) составляет в среднем 0,046 % (по массе) и 0,0314 % (по объему).
Углекислый газ вырабатывается в органах и тканях человека образуется в качестве одного из конечных продуктов метаболизма. Он переносится от тканей по венозной системе и затем выделяется с выдыхаемым воздухом через лёгкие. Таким образом, содержание углекислого газа в крови велико в венозной системе, уменьшается в капиллярной сети лёгких, и содержание его мало в артериальной крови. В выдыхаемом человеком воздухе содержится около 4,5% диоксида углерода, что в 60-110 раз больше, чем во вдыхаемом. Организм человека выделяет приблизительно 1 кг углекислого газа в сутки.
Углекислый газ растворяется в воде. В 100 граммах воды растворяется 0,3803 грамма CO2 при 16 °C, 0,3369 грамма CO2 – при 20 °C, 0,2515 грамма CO2 – при 30 °C. Растворяясь в воде, образует угольную кислоту Н2CO3. Растворим также в ацетоне, бензоле, метаноле и этаноле.
Термически устойчив при температурах менее 1000 °C. При температуре 1000 °C восстанавливается углем до оксида углерода (II).
При нормальном атмосферном давлении диоксид углерода не существует в жидком состоянии, существует только в твердом или газообразном состоянии. Твердая двуокись углерода при повышении температуры не плавится, а переходит (возгоняется) непосредственно из твёрдого состояния в газообразное. Твёрдую двуокись углерода также называют сухим льдом. Внешний вид сухого льда напоминает обычный лед, снегоподобную массу. При сублимации сухой лед поглощает около 590 кДж/кг (140 ккал/кг) теплоты.
Под давлением 35 000 атм. твердая углекислота становится проводником электрического тока.
Жидкий углекислый газ можно получить при повышении давления. Так, при температуре 20 °С и давлении свыше 6 МПа (~60 атм.) газ сгущается в бесцветную жидкость. При нормальных условиях (20 °С и 101,3 кПа) при испарении 1 кг жидкой углекислоты образуется 509 л углекислого газа. Хранят и транспортируют углекислый газ, как правило, в жидком состоянии
Двуокись углерода негорюча, но в ее атмосфере может поддерживаться горение активных металлов, например, щелочных металлов и щелочноземельных – магния, кальция, бария.
Двуокись углерода нетоксична, невзрывоопасна.
Предельно допустимая концентрация двуокиси углерода в воздухе рабочей зоны не установлена, при оценке этой концентрации можно ориентироваться на нормативы для угольных и озокеритовых шахт, установленные в пределах 0,5% (об.) или 9,2 г/м (см. ГОСТ 8050-85 «Двуокись углерода газообразная и жидкая. Технические условия»).
По степени воздействия на организм человека двуокись углерода относится к 4-му классу опасности по ГОСТ 12.1.007-76.
При концентрациях более 5% (92 г/м) двуокись углерода оказывает вредное влияние на здоровье человека, так как она тяжелее воздуха в полтора раза и может накапливаться в слабопроветриваемых помещениях у пола и в приямках, а также во внутренних объемах оборудования для получения, хранения и транспортирования газообразной, жидкой и твердой двуокиси углерода. При этом снижается объемная доля кислорода в воздухе, что может вызвать явление кислородной недостаточности и удушья.
Углекислый газ образуется при гниении и горении органических веществ, в результате вулканической деятельности. Содержится в воздухе и минеральных источниках, выделяется при дыхании животных и растений. Искусственными источниками образования углекислого газа являются промышленные выбросы и выхлопные газы автомобильного транспорта.
Углекислый газ легко пропускает излучение в ультрафиолетовой и видимой частях спектра, которое поступает на Землю от Солнца и обогревает её. В то же время он поглощает испускаемое Землёй инфракрасное излучение и является одним из парниковых газов, вследствие чего участвует в процессе глобального потепления.
Углекислый газ и мы: чем опасен CO2
Углекислый газ — один из продуктов обмена веществ в организме человека. Он играет большую роль в управлении дыханием и снабжением кровью органов. Рост содержания CO2 в крови вызывает расширение сосудов, способных таким образом транспортировать больше кислорода к тканям и органам. Аналогично и система дыхания понуждается к большей активности, если концентрация углекислоты в организме растет. Это свойство используют в аппаратах искусственной вентиляции легких, чтобы подстегнуть собственные органы дыхания пациента к большей активности.
https://youtube.com/watch?v=DqbvEhn5uJc
Кроме упомянутой пользы, превышение концентрации СO2 может принести организму и вред. Повышенное содержание во вдыхаемом воздухе приводит к тошноте, головной боли, удушью и даже к потере сознания. Организм протестует против углекислого газа и подает человеку сигналы. При дальнейшем увеличении концентрации развивается кислородное голодание, или гипоксия. Co2 мешает кислороду присоединяться к молекулам гемоглобина, которые и осуществляют перемещение связанных газов по кровеносной системе. Кислородное голодание ведет к снижению работоспособности, ослаблению реакции и способностей к анализу ситуации и принятию решений, апатии и может привести к смерти.

Общие симптомы отравления углекислым газом
Такие концентрации углекислого газа, к сожалению, достижимы не только в тесных шахтах, но и в плохо проветриваемых школьных классах, концертных залах, офисных помещениях и транспортных средствах — везде, где в замкнутом пространстве без достаточного воздухообмена с окружающей средой скапливается большое количество людей.
Поглотители двуокиси углерода
Поглотителями называют любые искусственные или природные системы, которые впитывают из воздуха углекислый газ. Поглотитель — это структура, которая вбирает из воздуха больше CO2 чем выбрасывает в него.
Природные поглотители
Леса способны воздействовать на количество двуокиси углерода в воздухе. Они могут быть и поглотителями, и источниками выбросов параллельно (при вырубке). Когда деревья увеличиваются, а лес растет, то углекислый газ поглощается. Данный процесс считается основой развития биомассы. Выходит, что прогрессирующий лес выступает поглотителем.

Лес северного полушария
При сжигании и уничтожении леса основная доля накопленного углерода опять преобразуется в углекислый газ. В итоге лес снова является источником СО2. Фитопланктон также является поглотителем углекислого газа на земле. При этом большая часть поглощенного углерода, передаваясь по пищевой цепочке, остается в океане.
Искусственные поглотители
Самыми известными поглотителями СО2 считаются: раствор едкого калия, натронная известь и асбест, едкий натр. Эти соединения при протекании химических реакций связывают углекислоту, преобразовывая ее в другие соединения. Существуют установки, которые улавливают углекислый газ из выбросов электростанций и преобразуют его в жидкое или твердое состояние с последующим применением в промышленности. Производятся испытания закачки углекислого газа, растворенного в воде, в базальтовые породы под землей. В процессе реакции образуется твердый минерал.

Станция закачки углекислого газа под землю
Химические и биологические свойства углекислого газа
Углекислый газ обладает кислотными свойствами, так как является кислотным оксидом, и при растворении в воде образует угольную кислоту:
CO₂+H₂O=H₂CO₃
Вступает в реакцию со щелочами, в результате чего образуются карбонаты и гидрокарбонаты. Этот газ не подвержен горению. В нем горят только некоторые активные металлы, например, магний.
При нагревании углекислый газ распадается на угарный газ и кислород:
2CO₃=2CO+O₃.
Как и другие кислотные оксиды, данный газ легко вступает в реакцию с другими оксидами:
СaO+Co₃=CaCO₃.
Углекислый газ входит в состав всех органических веществ. Круговорот этого газа в природе осуществляется с помощью продуцентов, консументов и редуцентов. В процессе жизнедеятельности человек вырабатывает примерно 1 кг углекислого газа в сутки. При вдохе мы получаем кислород, однако в этот момент в альвеолах образуется углекислый газ. В этот момент происходит обмен: кислород попадает в кровь, а углекислый газ выходит наружу.
Получение углекислого газа происходит при производстве алкоголя. Также этот газ является побочным продуктом при получении азота, кислорода и аргона. Применение углекислого газа необходимо в пищевой промышленности, где углекислый газ выступает в качестве консерванта, а также углекислый газ в виде жидкости содержится в огнетушителях.
Цели:
Расширить представления об истории открытия, свойствах и практическом применении углекислого газа.
Познакомить учащихся с лабораторными способами получения углекислого газа.
Продолжить формирование экспериментальных навыков учащихся.
Используемые приемы:
“верные и неверные утверждения”, “зигзаг-1”, кластеры.
Лабораторное оборудование:
лабораторный штатив, прибор для получения газов, стакан на 50 мл, кусочки мрамора, соляная кислота (1:2), известковая вода, зажим Мора.
I. Стадия вызова
На стадии вызова используется прием “верные и неверные утверждения”.
| Утверждения |
II. Стадия осмысления
1. Организация деятельности в рабочих группах, участники которых получают тексты по пяти основным темам “зигзага”:
- История открытия углекислого газа
- Углекислый газ в природе
- Получение углекислого газа
- Свойства углекислого газа
- Практическое применение углекислого газа
Идет первоначальное знакомство с текстом, первичное чтение.
2. Работа в экспертных группах.
В экспертные группы объединяются “специалисты” по отдельным вопросам. Их задача – внимательное чтение текста, выделение ключевых фраз и новых понятий либо использование кластеров и различных схем для графического изображения содержания текста (работа ведется индивидуально).
3. Отбор материала, его структурирование и дополнение (групповая работа)
4. Подготовка к трансляции текста в рабочих группах
- 1-я группа экспертов составляет опорный конспект “История открытия углекислого газа”
- 2-я группа экспертов составляет схему распространения углекислого газа в природе
- 3-я группа экспертов составляет схему получения углекислого газа и рисунок установки для его получения
- 4-я группа экспертов составляет классификацию свойств углекислого газа
- 5-я группа экспертов составляет схему практического применения углекислого газа
5. Подготовка к презентации (плакат)
III. Стадия рефлексии
Возвращение в рабочие группы
- Трансляция в группе тем 1–5 последовательно. Сбор установки для получения углекислого газа. Получение углекислого газа и исследование его свойств.
- Обсуждение результатов эксперимента.
- Презентация отдельных тем.
- Возвращение к “верным и неверным утверждениям”. Проверка своих первоначальных предположений. Расстановка новых значков.
Это может выглядеть так:
| Утверждения |
| 1. Углекислый газ – это “дикий газ”. |
| 2. В морях и океанах содержится в 60 раз больше углекислого газа, чем в земной атмосфере. |
| 3. Природные источники углекислого газа называются мофетами. |
| 4. В окрестностях Неаполя находится “Собачья пещера”, в которой не могут находиться собаки. |
| 5. В лабораториях углекислый газ получают действием серной кислоты на куски мрамора. |
| 6. Углекислый газ – это газ без цвета и запаха, легче воздуха, хорошо растворим в воде. |
| 7. Твёрдый углекислый газ получил название “сухого льда”. |
| 8. Известковая вода – это раствор гидроксида кальция в воде. |
Методы регистрации
Измерение парциального давления углекислого газа требуется в технологических процессах, в медицинских применениях — анализ дыхательных смесей при искусственной вентиляции лёгких и в замкнутых системах жизнеобеспечения. Анализ концентрации CO2 в атмосфере используется для экологических и научных исследований, для изучения парникового эффекта.
Углекислый газ регистрируют с помощью газоанализаторов основанных на принципе инфракрасной спектроскопии и других газоизмерительных систем. Медицинский газоанализатор для регистрации содержания углекислоты в выдыхаемом воздухе называется капнограф.
| Углекислый газ | |
| Общие | |
| Систематическое наименование | |
| Традиционные названия | углекислый газ, двуокись углерода, сухой лёд (в твёрдом состоянии) |
| Химическая формула | CO2 |
| Физические свойства | |
| Состояние | бесцветный газ |
| Молярная масса | 44,01 г/моль |
| Плотность | газ 1,9768 0 кг/м³ ж. 925 0°С, 35,5 ат кг/м³ тв. 1560 -78,5 кг/м³ |
| Динамическая вязкость | 8,5·10 -5 Па·с (10°C; 5,7 МПа) |
| Термические свойства | |
| Т. субл. | -78,5 °C |
| Тройная точка | -56,6°C; 0,52 МПа |
| Кр. точка | 31,1 °C; 7,38 МПа |
| Уд. теплоёмк. | 846 Дж/(кг·К) |
| Удельная теплота плавления | 25,13 кДж/моль |
| Химические свойства | |
| Растворимость в воде | 1,45 кг/м³ |
| Классификация | |
| Рег. номер CAS | 124-38-9 |
| RTECS | FF6400000 |
| Безопасность | |
| S-фразы | S9 , S23 , S36 |
| Приводятся данные для стандартных условий (25 °C, 100 кПа), если не указано иного. |
Диоксид углерода
(оксид углерода (IV), углекислый газ, CO2) — прочное химическое соединение, распространено в природных газах, содержащих его в количестве от нескольких процентов до практически чистого углекислого газа. Конечный продукт окисления углерода, не горит, не поддерживает горения и дыхания. Токсическое действие углекислого газа оказывается при его содержании в воздухе 3-4 % и заключается в раздражении дыхательных путей, головокружении, головной боли, шуме в ушах, психическом возбуждении, бессознательном состоянии.
Основные достоинства и недостатки пожаротушения углекислотой CO2
Главными преимуществами являются:
- Безопасность для любых материалов;
- Простота в эксплуатации;
- Возможность использования на любых объектах, в том числе содержащие электрическое оборудование, находящееся под напряжением;
- Использование специальных окрашивающих и одорирующих добавок к основному компоненту пожаротушения углекислотой СО2;
- Эффективность при кратко- и среднесрочном применении.
Основные «минусы», которые необходимо учитывать при применении, следующие:
- Потенциальная угроза находящимся в обслуживаемом помещении людям из-за критичного недостатка кислорода при пожаротушении CO2. Максимально допустимое содержание углекислого газа в окружающем воздухе для пребывания человека – 10%, при этом пожаротушащий эффект наступает при 30%, поэтому оперативную эвакуацию людей из обслуживаемых помещений необходимо произвести очень быстро;
- Максимальная эффективность пожаротушения углекислотой СО2 наступает при локализации крупных возгораний, при этом для тушения более мелких объектов локализации пожаров лучше применять другие средства.
Скачать: Варианты построения модулей и батарей с баллонами LPG:
- Техническое описание. Руководство по эксплуатации и техническому обслуживанию.
- Инструкция по установке и демонтажу соленоидного и ручного клапана на запорно-пусковое устройстве LPG-128.
- English. Installation, maintenance and user manual for carbon dioxide (CO2) fire extinguishing system.
- English. Technical instruction.
- English. Technical instruction. Disasemling solenoid valve LPG.
Применение
Пищевая добавка Е290 применяется в производстве газированных напитков, в составе разрыхлителя для теста, выпечки и кондитерских изделий, при заморозке свежих продуктов, мороженного.
В криохирургии используется как одно из основных веществ для криоабляции новообразований.
Жидкая углекислота широко применяется в системах пожаротушения и в огнетушителях. Автоматические углекислотные установки для пожаротушения различаются по системам пуска, которые бывают пневматическими, механическими или электрическими.
Устройство для подачи углекислого газа в аквариум может включать в себя резервуар с газом. Простейший и наиболее распространенный метод получения углекислого газа основан на конструкции для изготовления алкогольного напитка браги. При брожении, выделяемый углекислый газ вполне может обеспечить подкормку аквариумных растений.
Углекислый газ используется для газирования лимонада и газированной воды. Углекислый газ используется также в качестве защитной среды при сварке проволокой, но при высоких температурах происходит его распад с выделением кислорода. Выделяющийся кислород окисляет металл. В связи с этим приходится в сварочную проволоку вводить раскислители, такие как марганец и кремний. Другим следствием влияния кислорода, также связанного с окислением, является резкое снижение поверхностного натяжения, что приводит, среди прочего, к более интенсивному разбрызгиванию металла, чем при сварке в инертной среде.
Углекислота в баллончиках применяется в пневматическом оружии (в газобаллонной пневматике) и в качестве источника энергии для двигателей в авиамоделировании.
Хранение углекислоты в стальном баллоне в сжиженном состоянии выгоднее, чем в виде газа. Углекислота имеет сравнительно низкую критическую температуру +31 °С. В стандартный 40-литровый баллон заливают около 30 кг сжиженного углекислого газа, и при комнатной температуре в баллоне будет находиться жидкая фаза, а давление составит примерно 6 МПа (60 кгс/см2). Если температура будет выше +31 °С, то углекислота перейдёт в сверхкритическое состояние с давлением выше 7,36 МПа. Стандартное рабочее давление для обычного 40-литрового баллона составляет 15 МПа (150 кгс/см2), однако он должен безопасно выдерживать давление в 1,5 раза выше, то есть 22,5 МПа, — таким образом, работа с подобными баллонами может считаться вполне безопасной.
Твёрдая углекислота — «сухой лёд» — используется в качестве хладагента в лабораторных исследованиях, в розничной торговле, при ремонте оборудования (например: охлаждение одной из сопрягаемых деталей при посадке внатяг) и т. д. Для сжижения углекислого газа и получения сухого льда применяются углекислотные установки.
Польза и вред
Е290 считается нетоксичным (4 класс опасности ГОСТ 12.1.007), но при вдыхании диоксида углерода в повышенных концентраций в воздухе по воздействию на воздуходышащие живые организмы его относят к удушающим газам.
Незначительные повышения концентрации, вплоть до 2–4 %, в помещениях приводят к развитию у людей сонливости и слабости. Опасными для здоровья концентрациями считаются концентрации около 7–10 %, при которых развиваются симптомы удушья, проявляющиеся в виде головной боли, головокружения, расстройстве слуха и в потере сознания (симптомы, сходные с симптомами высотной болезни), эти симптомы развиваются, в зависимости от концентрации, в течение времени от нескольких минут до одного часа.
При вдыхании воздуха с очень высокими концентрациями газа смерть наступает очень быстро от удушья, вызванного гипоксией.
Несмотря на то, что даже концентрация 5–7 % CO₂ в воздухе несмертельна, но при концентрации 0,1 % (такое содержание углекислого газа иногда наблюдается в воздухе мегаполисов), люди начинают чувствовать слабость, сонливость. Это показывает, что даже при высоком уровне кислорода, большая концентрация CO2 существенно влияет на самочувствие человека.
Токсичность
Углекислый газ нетоксичен, но по воздействию его повышенных концентраций в воздухе на воздуходышащие живые организмы его относят к удушающим газам (англ.)русск.. Незначительные повышения концентрации до 2-4 % в помещениях приводят к развитию у людей сонливости и слабости. Опасными концентрациями считаются уровни около 7-10 %, при которых развивается удушье, проявляющее себя в головной боли, головокружении, расстройстве слуха и в потере сознания (симптомы, сходные с симптомами высотной болезни), в зависимости от концентрации, в течение времени от нескольких минут до одного часа. При вдыхании воздуха с высокими концентрациями газа смерть наступает очень быстро от удушья.
Хотя, фактически, даже концентрация 5-7 % CO2 не смертельна, уже при концентрации 0,1 % (такое содержание углекислого газа наблюдается в воздухе мегаполисов) люди начинают чувствовать слабость, сонливость. Это показывает, что даже при высоких содержаниях кислорода большая концентрация CO2 сильно влияет на самочувствие.
Вдыхание воздуха с повышенной концентрацией этого газа не приводит к долговременным расстройствам здоровья и после удаления пострадавшего из загазованной атмосферы быстро наступает полное восстановление здоровья.
